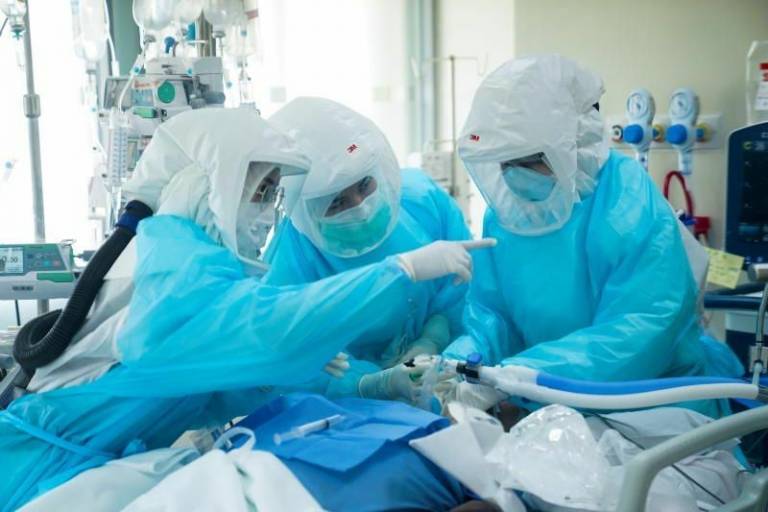
ผู้ควบคุมยาเสพติดของสหภาพยุโรปกล่าวว่า อาจมีการตัดสินใจภายในระยะเวลาไม่กี่สัปดาห์ ว่าจะมีการอนุมัติการใช้ยา Paxlovid ของไฟเซอร์สำหรับ COVID-19 หรือไม่ หลังจากที่ผู้ผลิตยาสหรัฐยื่นคำขอขออนุญาต สำนักงานยาแห่งยุโรป (European Medicines Agency) ระบุว่า การขออนุมัติดังกล่าว มีไว้เพื่อการรักษาโรคติดเชื้อไวรัสโควิด-19 ในระดับเล็กน้อยถึงปานกลาง ในผู้ป่วยที่มีอายุ 12 ปีขึ้นไป ซึ่งมีน้ำหนักอย่างน้อย 40 กิโลกรัม และมีความเสี่ยงสูงที่อาการป่วยจะแย่ลง แม้ว่าวัคซีนจะเป็นหัวใจสำคัญในการต่อสู้กับการแพร่ระบาด แต่หน่วยงานกำกับดูแลมองว่าการรักษาเป็นเครื่องมือใหม่ในการต่อต้านเชื้อ Omicron ที่แพร่ระบาดอย่างรวดเร็ว ซึ่งขณะนี้มีการตรวจพบในกว่า 128 ประเทศทั่วโลก ยาของไฟเซอร์ Paxlovid ตั้งใจจะให้ผู้ป่วยนำกลับบ้านเป็นเวลา 5 วัน หลังจากเริ่มมีอาการติดเชื้อ COVID-19 ได้รับอนุญาตสำหรับผู้ที่มีอายุ 12 ปีขึ้นไป โดยสำนักงานคณะกรรมการอาหาร และยาแห่งสหรัฐอเมริกาในเดือนธันวาคม
ในการทดลองทางคลินิก เกือบร้อยละ 90 มีประสิทธิภาพในการป้องกันการรักษาในโรงพยาบาล และการเสียชีวิตในผู้ป่วยที่มีความเสี่ยงสูงที่จะเจ็บป่วยรุนแรง